LEMTRADA (ALEMTUZUMAB) DOKTOR MEKTUBU
Sağlık Bakanlığı Türkiye İlaç ve Tıbbî Cihaz Kurumu tarafından Lemtrada (Alemtuzumab) doktor mektubu yayımlandı.

27 Ağustos 2019 Salı 16:04
26.08.2019
▼ LEMTRADA (ALEMTUZUMAB): CİDDİ GÜVENLİLİK ENDİŞELERİ
NEDENİYLE KULLANIMININ KISITLANMASI
Sayın Sağlık Mesleği Mensubu,
Bu mektubun amacı, Lemtrada kullanımı sonucu ortaya çıkan ciddi güvenlilik endişeleri hakkında sizi bilgilendirmektir.
Avrupa İlaç Ajansı (EMA), Lemtrada (alemtuzumab) kullanımını takiben ciddi kardiyovasküler reaksiyonlar, yeni tanımlanan otoimmün hepatit ve hemofagositik lenfohistiyositoz bildirilmesi üzerine söz konusu ilacın Multiple Skleroz tedavisindeki yararlarını ve risklerini yeniden gözden geçirmektedir.
Bu mektuba https://www.titck.gov.tr/ adresinden de ulaşabilirsiniz.
Değerlendirme tamamlanıncaya kadar aşağıdaki önlemlerin alınması gerekmektedir:
Özet
• Yeni tedavi, yalnızca en az iki hastalık modifiye edici tedaviyle tam ve yeterli bir tedavi süresine rağmen yüksek derecede aktif relaps remitting multipl sklerozu olan yetişkinlerde veya tüm diğer hastalık modifiye edici tedavilerin kontrendike olduğu veya uygun olmadığı yüksek derecede aktif relaps remitting multiple sklerozu olan yetişkinlerde başlatılmalıdır.
• Lemtrada ile tedavi edilen hastalarda intravenöz infüzyon öncesi ve sırasında kan basıncı da dahil olmak üzere yaşamsal belirtiler izlenmelidir. Klinik olarak önemli değişiklikler gözlenirse, infüzyonun kesilmesi ve EKG de dahil olmak üzere ek izleme yapılması göz önünde bulundurulmalıdır.
• Karaciğer fonksiyon testleri tedavi öncesi ve sırasında yapılmalıdır. Hastalarda karaciğerde hasar belirtileri, açıklanamayan karaciğer enzim yükselmeleri veya hepatik disfonksiyonu gösteren belirtiler (örn; açıklanamayan mide bulantısı, kusma, karın ağrısı, yorgunluk, iştahsızlık, sarılık veya koyu renkli idrar) gelişirse, yalnızca dikkatli bir şekilde değerlendirildikten sonra Lemtrada tekrar uygulanmalıdır.
• Patolojik immün aktivasyon belirtileri gelişen hastalar derhal değerlendirilmeli ve hemofagositik lenfohistiyositoz tanısı düşünülmelidir. İmmün aktivasyon belirtileri, tedavinin başlamasından sonraki dört yıla kadar ortaya çıkabilir.
• Hastalar, infüzyonu takiben birkaç gün içinde gelişebilecek belirtilerde ve hepatik hasar belirtisi ortaya çıkması durumunda derhal hekimlerine başvurmaları konusunda bilgilendirilmelidirler.
Güvenlilik sorunu üzerine ayrıntılı bilgiler
EMA Lemtrada’nın onaylı endikasyonunda yarar/risk dengesini tekrar değerlendirmeye başlamıştır. Bunun nedeni; ilacın pazarlama sonrası kullanımı ile fatal olgular, infüzyonlar ile yakın zamansal ilişkisi bulunan kardiyovasküler advers olaylar ve immün aracılı advers reaksiyonlar da dahil olmak üzere ciddi güvenlilik endişelerinin ortaya çıkmasıdır.
Ortaya çıkan bu pazarlama sonrası veriler ışığında, alemtuzumabın aşağıdaki durumlarla ilişkili olduğu düşünülmektedir:
Otoimmün hepatit ve karaciğer hasarı
Alemtuzumab ile tedavi edilen hastalarda serum transaminaz artışları ve otoimmün hepatiti de içeren (fatal olgular dahil olmak üzere) karaciğer hasarı olguları bildirilmiştir. Karaciğer fonksiyonu, tedaviye başlamadan önce ve tedavi sırasında değerlendirilmelidir. Hastalar; karaciğer hasarı riski ve bununla ilişkili olarak bulantı, kısma, karın ağrısı, yorgunluk, iştah kaybı, deride ve gözlerde sararma veya idrarda koyulaşma ya da normalden daha kolay kanama veya morarma gibi semptomlar hakkında bilgilendirilmelidir. Bu bulguların ortaya çıkması durumunda, tedavi yalnızca, dikkatli bir değerlendirmeyi takiben tekrarlanmalıdır.
Alemtuzumab infüzyonu ile geçici olarak ilişkilendirilen diğer ciddi reaksiyonlar
Pazarlama sonrası kullanım sırasında pulmoner alveolar hemoraji, miyokard infarktüsü, inme (iskemik ve hemorajik inme dahil olmak üzere) ve servikosefalik (örn; vertebral ve karotis) arter diseksiyonu olguları bildirilmiştir. Reaksiyonlar, tedavi sırasında herhangi bir dozu takiben ortaya çıkabilmektedir. Olguların çoğunda reaksiyonlar, infüzyondan itibaren 1-3 gün içinde ortaya çıkmıştır. Hastalara bu olaylara ilişkin belirti ve bulgular hakkında bilgi verilmeli ve bu bulgulardan herhangi birinin gelişmesi durumunda derhal tıbbi yardım için başvurmaları tavsiye edilmelidir.
Lemtrada infüzyonundan önce ve infüzyon sırasında, kan basıncı da dahil olmak üzere yaşamsal belirtiler periyodik olarak izlenmelidir. Yaşamsal belirtilerde klinik açıdan önemli değişikliklerin gözlenmesi halinde, infüzyonun durdurulması ve EKG de dahil olmak üzere ek izlem düşünülmelidir.
Hemofagositik lenfohistiyositoz
Pazarlama sonrası kullanım sırasında, Lemtrada ile tedavi edilen hastalarda hemofagositik lenfohistiyositoz bildirilmiştir. Hemofagositik lenfohistiyositoz ateş, lenf nodlarında şişme, morarma ve deride döküntüyü içeren aşırı sistemik enflamasyona ilişkin klinik belirti ve bulgularla karakterize olan ve yaşamı tehdit eden patolojik bir immün aktivasyon sendromudur. Erken teşhis ve tedavi edilmemesi halinde yüksek mortalite ile seyreder. Semptomların, tedavinin başlatılmasını takiben birkaç ay ila dört yıl arasında ortaya çıktığı bildirilmiştir. Patolojik immün aktivasyona ilişkin hastalık manifestasyonlarının geliştiği hastalar derhal değerlendirmeye alınmalı ve hemofagositik lenfohistiyositoz tanısı düşünülmelidir.
Bildirim gerekliliği
Lemtrada reçete edilirken yukarıda belirtilen hususlara dikkat edilmesini ve söz konusu ilacın kullanımı sırasında advers reaksiyon oluşması durumunda T.C. Sağlık Bakanlığı, Türkiye İlaç ve Tıbbi Cihaz Kurumu, Farmakovijilans ve Kontrole Tabi Maddeler Dairesi, Türkiye Farmakovijilans Merkezi'ni (TÜFAM) (e-posta: [email protected]; tel: 0 800 314 00 08; faks: 0 312 218 35 99) bilgilendirmenizi hatırlatırız.
Saygılarımızla,
Sağlık Bakanlığı
Türkiye İlaç ve Tıbbi Cihaz Kurumu
▼ Bu ilaç ek izlemeye tabidir. Bu üçgen yeni güvenlilik bilgisinin hızlı olarak belirlenmesini sağlayacaktır. Sağlık mesleği mensuplarının şüpheli advers reaksiyonlarını bildirmeleri beklenmektedir. Raporlama yapılması, ilacın yarar/risk dengesinin sürekli olarak izlenmesine olanak sağlamaktadır.
Sağlık Aktüel - www.saglikaktuel.com
YASAL UYARI: Yayınlanan köşe yazısı/haberin tüm hakları Sağlık Aktüel’e (www.saglikaktuel.com) aittir. www.saglikaktuel.com biçiminde aktif bağlantı kurulabilir, açık kaynak gösterilmek kaydıyla içerik kullanılabilir. Açık kaynak göstermeden yapılan alıntılar için yasal işlem uygulanacaktır.
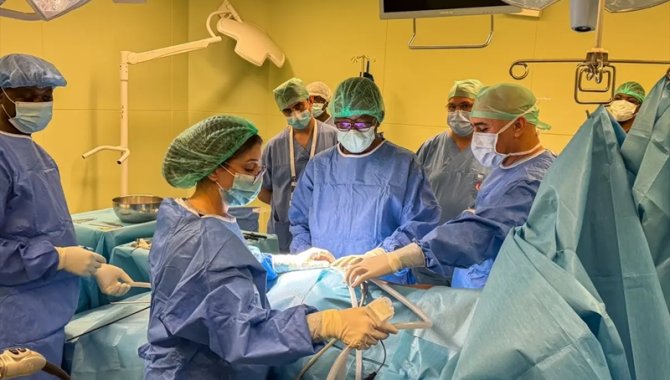
![Başakşehir Çam ve Sakura’da Kapalı Yöntemle 3 Damar Bypass Ameliyatı]() Başakşehir Çam ve Sakura’da Kapalı Yöntemle 3 Damar Bypass Ameliyatıİstanbul’da göğüs ağrısı şikayetiyle hastaneye başvuran Murat Zengi’nin 3 damarının tıkalı olduğu belirlendi. Başakşehir Çam ve Sakura Şehir Hastanesi’nde gerçekleştirilen minimal invaziv bypass ameliyatıyla hasta, göğüs kafesi açılmadan sağlığına kavuştu20 Mayıs 2026 Çarşamba 16:35BASIN HABERLERİ
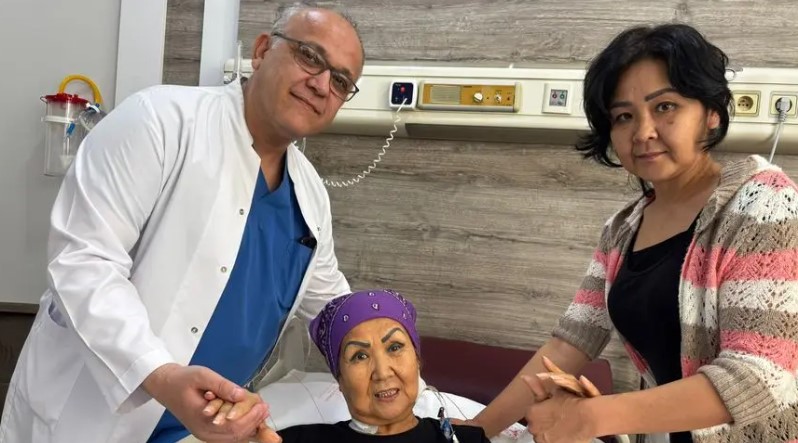
Başakşehir Çam ve Sakura’da Kapalı Yöntemle 3 Damar Bypass Ameliyatıİstanbul’da göğüs ağrısı şikayetiyle hastaneye başvuran Murat Zengi’nin 3 damarının tıkalı olduğu belirlendi. Başakşehir Çam ve Sakura Şehir Hastanesi’nde gerçekleştirilen minimal invaziv bypass ameliyatıyla hasta, göğüs kafesi açılmadan sağlığına kavuştu20 Mayıs 2026 Çarşamba 16:35BASIN HABERLERİ![Kazak Hasta Antalya’da Kapalı Kalp Ameliyatıyla Sağlığına Kavuştu]() Kazak Hasta Antalya’da Kapalı Kalp Ameliyatıyla Sağlığına KavuştuKazakistan’da yıllardır kalp rahatsızlığı yaşayan Ulbossın Sartayeva, Antalya’da gerçekleştirilen minimal invaziv kalp kapak değişimi ameliyatıyla yeniden sağlığına kavuştu. Başarılı operasyon meme altından yapılan 6 santimetrelik kesiyle gerçekleştirildi20 Mayıs 2026 Çarşamba 16:27BASIN HABERLERİ
Kazak Hasta Antalya’da Kapalı Kalp Ameliyatıyla Sağlığına KavuştuKazakistan’da yıllardır kalp rahatsızlığı yaşayan Ulbossın Sartayeva, Antalya’da gerçekleştirilen minimal invaziv kalp kapak değişimi ameliyatıyla yeniden sağlığına kavuştu. Başarılı operasyon meme altından yapılan 6 santimetrelik kesiyle gerçekleştirildi20 Mayıs 2026 Çarşamba 16:27BASIN HABERLERİ![Sağlık Raporlarında Yeni Dönem: e-Nabız Üzerinden Başvuru Dönemi Başladı]() Sağlık Raporlarında Yeni Dönem: e-Nabız Üzerinden Başvuru Dönemi BaşladıSağlık Bakanlığı’nın yürürlüğe koyduğu yeni yönetmelikle sağlık raporu işlemlerinde dijital dönem başladı. Başvurular artık e-Nabız üzerinden yapılacak, hastanelerde ise “Rapor Başvuru Merkezi” kurulacak.20 Mayıs 2026 Çarşamba 16:24BASIN HABERLERİ
Sağlık Raporlarında Yeni Dönem: e-Nabız Üzerinden Başvuru Dönemi BaşladıSağlık Bakanlığı’nın yürürlüğe koyduğu yeni yönetmelikle sağlık raporu işlemlerinde dijital dönem başladı. Başvurular artık e-Nabız üzerinden yapılacak, hastanelerde ise “Rapor Başvuru Merkezi” kurulacak.20 Mayıs 2026 Çarşamba 16:24BASIN HABERLERİ![DSÖ’den Kongo’daki Ebola Salgını İçin Kritik Uyarı: Vaka Sayısı Artıyor]() DSÖ’den Kongo’daki Ebola Salgını İçin Kritik Uyarı: Vaka Sayısı ArtıyorDünya Sağlık Örgütü, Kongo Demokratik Cumhuriyeti’nde görülen Ebola salgınının ciddi boyutlara ulaştığını açıkladı. Yetkililer, yüzlerce şüpheli vaka ve artan can kayıpları nedeniyle gözetim ve sınır önlemlerini artırıyor.20 Mayıs 2026 Çarşamba 16:22BASIN HABERLERİ
DSÖ’den Kongo’daki Ebola Salgını İçin Kritik Uyarı: Vaka Sayısı ArtıyorDünya Sağlık Örgütü, Kongo Demokratik Cumhuriyeti’nde görülen Ebola salgınının ciddi boyutlara ulaştığını açıkladı. Yetkililer, yüzlerce şüpheli vaka ve artan can kayıpları nedeniyle gözetim ve sınır önlemlerini artırıyor.20 Mayıs 2026 Çarşamba 16:22BASIN HABERLERİ![Muş’ta Meslek Lisesi Öğrencilerinden Köy Okullarına İlk Yardım ve Hijyen Eğitimi]() Muş’ta Meslek Lisesi Öğrencilerinden Köy Okullarına İlk Yardım ve Hijyen EğitimiMuş’ta sağlık bölümü öğrencileri ve öğretmenleri, köy okullarındaki çocuklara ilk yardım, Heimlich manevrası ve kişisel hijyen konusunda uygulamalı eğitim verdi. Proje kapsamında 1000 öğrenciye ulaşılması hedefleniyor.20 Mayıs 2026 Çarşamba 16:20BASIN HABERLERİ
Muş’ta Meslek Lisesi Öğrencilerinden Köy Okullarına İlk Yardım ve Hijyen EğitimiMuş’ta sağlık bölümü öğrencileri ve öğretmenleri, köy okullarındaki çocuklara ilk yardım, Heimlich manevrası ve kişisel hijyen konusunda uygulamalı eğitim verdi. Proje kapsamında 1000 öğrenciye ulaşılması hedefleniyor.20 Mayıs 2026 Çarşamba 16:20BASIN HABERLERİ![Ankara Merkezli FETÖ Operasyonunda 24 Şüpheli Hakkında Gözaltı Kararı]() Ankara Merkezli FETÖ Operasyonunda 24 Şüpheli Hakkında Gözaltı KararıAnkara merkezli 11 ilde düzenlenen FETÖ operasyonunda, örgütün kamu mahrem yapılanması içerisinde faaliyet yürüttüğü öne sürülen 24 şüpheli hakkında gözaltı kararı verildi.20 Mayıs 2026 Çarşamba 16:17BASIN HABERLERİ
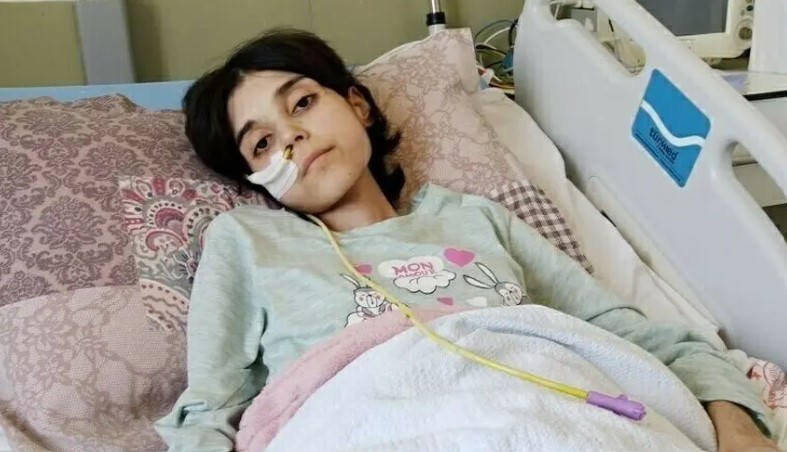
Ankara Merkezli FETÖ Operasyonunda 24 Şüpheli Hakkında Gözaltı KararıAnkara merkezli 11 ilde düzenlenen FETÖ operasyonunda, örgütün kamu mahrem yapılanması içerisinde faaliyet yürüttüğü öne sürülen 24 şüpheli hakkında gözaltı kararı verildi.20 Mayıs 2026 Çarşamba 16:17BASIN HABERLERİ![İzmir’de 17 Yaşındaki Ünzile Naz, Hayata Tutunmak İçin Destek Bekliyor]() İzmir’de 17 Yaşındaki Ünzile Naz, Hayata Tutunmak İçin Destek Bekliyorİzmir’in Torbalı ilçesinde yaşayan 17 yaşındaki Ünzile Naz Gümüştaş, geçirdiği bağırsak ameliyatının ardından gelişen sağlık sorunları nedeniyle yaşam mücadelesi veriyor.20 Mayıs 2026 Çarşamba 15:44BASIN HABERLERİ
İzmir’de 17 Yaşındaki Ünzile Naz, Hayata Tutunmak İçin Destek Bekliyorİzmir’in Torbalı ilçesinde yaşayan 17 yaşındaki Ünzile Naz Gümüştaş, geçirdiği bağırsak ameliyatının ardından gelişen sağlık sorunları nedeniyle yaşam mücadelesi veriyor.20 Mayıs 2026 Çarşamba 15:44BASIN HABERLERİ![Bakan Memişoğlu’ndan Küresel Sumud Filosu Açıklaması]() Bakan Memişoğlu’ndan Küresel Sumud Filosu AçıklamasıKemal Memişoğlu, Gazze’ye insani yardım ulaştırmak amacıyla yola çıkan Küresel Sumud Filosu’na uluslararası sularda müdahale edilmesine tepki gösterdi.20 Mayıs 2026 Çarşamba 15:41BASIN HABERLERİ
Bakan Memişoğlu’ndan Küresel Sumud Filosu AçıklamasıKemal Memişoğlu, Gazze’ye insani yardım ulaştırmak amacıyla yola çıkan Küresel Sumud Filosu’na uluslararası sularda müdahale edilmesine tepki gösterdi.20 Mayıs 2026 Çarşamba 15:41BASIN HABERLERİ![Seyrantepe’de Hastanede Tedavi Gören Hasta Pencereden Düşerek Hayatını Kaybetti]() Seyrantepe’de Hastanede Tedavi Gören Hasta Pencereden Düşerek Hayatını KaybettiSeyrantepe’de bir hastanede tedavi gören Kudret Özcan, kaldığı servisin bulunduğu kattaki pencereden düşerek yaşamını yitirdi. Olayla ilgili soruşturma başlatıldı.20 Mayıs 2026 Çarşamba 15:39BASIN HABERLERİ
Seyrantepe’de Hastanede Tedavi Gören Hasta Pencereden Düşerek Hayatını KaybettiSeyrantepe’de bir hastanede tedavi gören Kudret Özcan, kaldığı servisin bulunduğu kattaki pencereden düşerek yaşamını yitirdi. Olayla ilgili soruşturma başlatıldı.20 Mayıs 2026 Çarşamba 15:39BASIN HABERLERİ![Şanlıurfa’da Mezarlıkta Bulunan Ceninlerle İlgili 4 Kişi Gözaltına Alındı]() Şanlıurfa’da Mezarlıkta Bulunan Ceninlerle İlgili 4 Kişi Gözaltına AlındıŞanlıurfa’da mezarlıkta bir varil içerisinde bulunan insan ceninleriyle ilgili yürütülen soruşturmada 4 kişi gözaltına alındı. Şüpheliler, adli kontrol şartıyla serbest bırakıldı.20 Mayıs 2026 Çarşamba 15:34BASIN HABERLERİ
Şanlıurfa’da Mezarlıkta Bulunan Ceninlerle İlgili 4 Kişi Gözaltına AlındıŞanlıurfa’da mezarlıkta bir varil içerisinde bulunan insan ceninleriyle ilgili yürütülen soruşturmada 4 kişi gözaltına alındı. Şüpheliler, adli kontrol şartıyla serbest bırakıldı.20 Mayıs 2026 Çarşamba 15:34BASIN HABERLERİ
- Geri
- Ana Sayfa
- Normal Görünüm
- © 2006 Sağlık Aktüel